식약처, 생물학적제제 등 품목허가․심사 규정 개정 시행

오늘(5일)부터 「생물학적제제 등의 품목허가․심사 규정」이 개정, 시행된다.
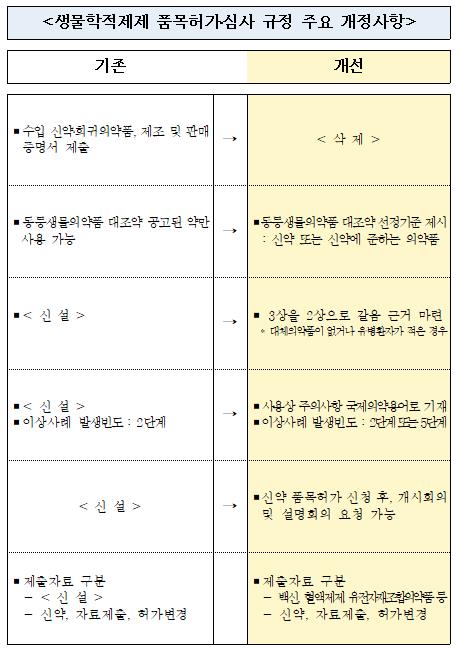
식품의약품안전처(처장 김강립)는 코로나19 백신 등 생물학적제제 등에 대한 신속한 허가․공급을 지원하기 위해 ▲수입 신약 및 희귀의약품 제출자료 간소화 ▲동등생물의약품 대조약 선정방식 개선 ▲임상시험 자료 합리화 ▲국제의약용어 우선 사용 등을 추진한다.
우선, 수입 신약 및 희귀의약품 허가 신청 서류 중 기존에 제출해야 했던 수출국 정부 당국 발행 ‘제조 및 판매증명서’ 제출을 면제한다. 이를 통해 감염병 대유행 예방․치료 의약품 등에 대해 식약처가 해외 규제당국의 허가여부와 별도로 평가, 신속한 허가 및 공급 지원이 기대된다.
또 동등생물의약품 대조약으로 공고된 의약품만 사용 가능한 것을 신약 및 신약에 준하는 의약품으로 제약사가 선정·사용할 수 있도록 선정기준을 제시했으며 대체의약품이 없거나 임상시험 대상 환자 수가 극히 적은 경우, 3상 임상시험을 2상 임상시험 자료로 갈음해 평가할 수 있는 법적 근거를 마련했다.
‘사용상의 주의사항’에는 국제의약용어(MedDRA)를 우선해 사용하도록 하고, 이상사례도 국제조화된 기준에 맞추어 용어와 발생빈도를 세분화해 환자와 의료 전문가에게 정확한 의료 정보를 제공할 수 있도록 개선했다.
아울러 신약 품목허가 신청 후 민원인이 허가․심사 담당부서에 설명회의 등을 요청할 수 있도록 ‘회의 신청제도’를 신설하고, 백신·혈액제제·유전자재조합의약품 등 제제별 특성을 반영해 품목허가 제출자료를 구체화했다.
저작권자 © 헬스이슈앤뉴스 무단전재 및 재배포 금지


