화이자, 모더나, 아스트라제네카, 얀센, 인도혈청연구소, 시노팜, 시노백, 바라트 등 8개 제품이 세계보건기구 긴급사용 승인 백신으로 사용되고 있는 가운데, 우리나라도 국내 첫 코로나19 백신 상용화를 위한 최종 임상평가에 착수했다.
질병관리청(청장 정은경) 국립보건연구원(원장 권준욱)은 국내 개발 코로나19 백신의 대규모 임상3상 시험 검체에 대한 효능평가(중화항체 분석)를 이번 주부터 시작한다고 21일 밝혔다.
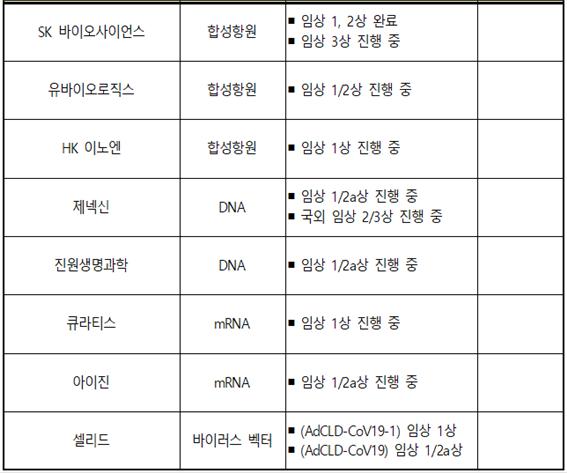
이번 효능평가 대상 백신은 현재 국내에서 임상시험 수행 중인 코로나19 백신 8개 가운데 임상 3상 중인 합성항원 백신으로, 내년 상반기 식품의약품안전처 품목 허가를 목표로 하고 있다.
그동안 국립보건연구원은 코로나19 백신의 국산화를 위해 공공백신개발지원센터를 중심으로 임상시험 검체 분석에 필수적인 기반시설과 인력을 확보, 지원해 왔다.
이번 임상3상 시험 결과의 공신력 확보를 위해 지난 8월 국립보건연구원과 국제백신연구소 간 업무협약을 체결하고 코로나19 백신의 중화항체 시험법에 대한 표준화 및 검증을 공동으로 진행했다.
이번 합성항원 백신 임상 3상 시험뿐만 아니라 국내 개발 DNA 백신의 임상 1/2상 시험의 효능평가를 지원 중이며, 앞으로 메신저리보핵산(mRNA) 백신 1상, 바이러스벡터 1/2상 임상검체 분석도 지속적으로 지원할 계획이다.
국립보건연구원 권준욱 원장은 “국내 첫 코로나19 백신의 상용화를 위한 마지막 단계이자 가장 중요한 과정이 시작됐다. 굳건한 민·관 공조체계를 통해 끝까지 최선을 다해 지원하겠다”고 밝혔다.
국제백신연구소 제롬 김 사무총장은 “검증된 시험법을 이용한 효능평가는 백신의 사용승인에서 필수적인 부분”이라며 “이 백신이 조속히 상용화되어 국내외에서 사용될 수 있도록 국립보건연구원 등과 협력할 것”이라고 말했다.