식약처, 긴급사용 승인 등 신속 대응으로 포스트 코로나 시대 준비
K-방역의 모범적 성과로 국내 개발 진단 시약의 국제적 수요가 증가한 것으로 나타났다. 20일 현재 73개 제품이 110여개국에 수출되고 있으며 특히 7개 제품은 미국 FDA의 긴급사용 승인을 받아 미국 등 해외로의 진출이 더욱 확대될 전망이다.
식품의약품안전처(처장 이의경)는 “그동안 긴급사용 승인 등 신속한 대응으로 K-방역 시스템 핵심인 코로나19 진단시약의 글로벌 위상이 높아졌다”고 평가하고 ∆긴급사용승인과 수출용 허가의 정식허가 전환 ∆진단시약 등 체외진단제품에 대한 체계적인 허가 지원 시스템 구축 ∆진단기법 등 국제 표준화 추진 등을 꼼꼼히 준비하면서 포스트 코로나 시대에도 K-방역의 명성을 확고히 하겠다는 의지를 나타냈다.

식약처는 코로나19 발발 이후 서류평가, 임상성능평가, 전문가 회의 등을 신속 진행함으로써 현재 총 6개의 제품이 긴급 승인됐다고 밝혔다.

국내 긴급사용 승인 6개 제품은 1일 최대 생산량 약 15만명분으로 20일 누적 총생산량은 150만명분으로 집계됐다. 이중 국내에는 131만명분이 공급되었고 지금까지 총 76만건의 검사를 진행했다. 현재 약 19만명분을 재고로 확보, 안정적인 수급을 이어가고 있다.
신속·모범적인 K-방역 성과는 진단시약의 국제적 수요 증가를 불러왔다. 5월 20일 기준, 73개 제품이 수출용으로 허가(유전자 50, 면역 23)되어 미국, 이탈리아, 브라질, 사우디아라비아, 이집트, 인도네시아 등 110여개국에 약 5646만명분의 진단시약이 수출되고 있다. 특히, 우리나라 진단시약 7개 제품은 미국 FDA의 긴급사용승인을 받아 미국 등으로의 진출이 더욱 확대될 것으로 전망된다.
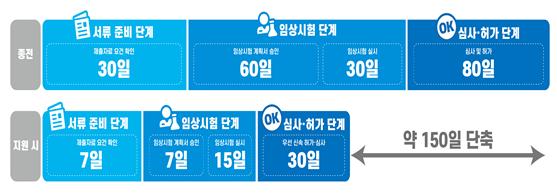
식약처는 긴급사용 승인 제품 및 수출용 허가 제품을 정식허가로 전환, 품질 신뢰도를 높일 계획이다. 특히 신청 준비단계부터 임상 시험단계, 심사·허가단계에 이르기까지 소요시간도 약 150일 단축키로 했다.
아울러 K-방역모델 국제표준화로 세계 방역시장을 선도하고 체외진단기기 특성에 맞춘 전주기 안전관리체계를 도입, ▲맞춤형 안전관리체계 구축 ▲전문성 강화 ▲기술지원을 통한 체외진단의료기기 안전성·유효성 및 산업 경쟁력 확보를 위한 정책을 추진할 예정이다.
식약처는 또 국내 진단시약의 품질관리에 필요한 표준품 제조‧관리‧분양, 국내외 기술정보, 최신 임상정보 등을 적기에 제공해 업계의 자체 품질 향상을 도모하고 임상적 성능시험 종사자는 전문교육을 이수토록 할 계획이다. 특히 체외진단 분야 핵심인재 양성을 위해 한국의료기기안전정보원의 규제과학전문가 교육과 연계, 인력 배출에도 주력키로 했다. 그리고 코로나19 진단에 사용되는 유전자증폭장치, 핵산추출시약 등 주요 체외진단 제품의 국산화가 가능하도록 범부처 전주기 의료기기 연구사업을 통해 적극 지원하기로 했다.


